O Brasil se prepara para iniciar outra fase de testes de uma possível vacina contra a Covid-19. Nesta segunda-feira (6), o governo de São Paulo anunciou que o imunizante será testado, em cooperação com Instituto Butantan, a partir do dia 20 de julho. Aliás, o recrutamento de voluntários começa já na próxima segunda-feira (13). Ainda assim, apenas profissionais de saúde poderão participar do estudo.

Leia Mais
Fundaj pede suspensão da construção do Atacadão no Poço da Panela
Ao todo, nove mil voluntários participarão dos testes em quatro estados – São Paulo, Rio Grande do Sul, Minas Gerais e Paraná – e no Distrito Federal. Além de serem profissionais da saúde, outros pré-requisitos são exigidos. É necessário, por exemplo, que os voluntários não tenham se contaminado pela Covid-19 anteriormente, que as mulheres não estejam grávidas ou planejem engravidar nos próximos três meses, e que os voluntários morem perto de um dos 12 centros de pesquisa que conduzirão o projeto.
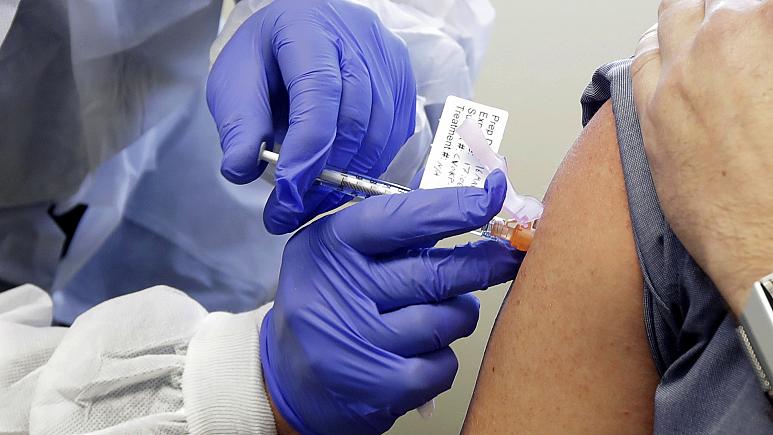
“No mundo são 136 vacinas em desenvolvimento, 12 em estudos clínicos. Desses 12, apenas 3 estão na fase chamada fase 3 (testes em humanos). Então, a partir da aprovação da Anvisa, nós nos credenciamos como uma das 3 vacinas que têm grande chance de chegar ao público muito rapidamente”, afirmou o diretor do Instituto Butantan, Dimas Covas. De acordo com o governo estadual, o Instituto Butantan está adaptando uma fábrica para a produção da vacina. Aliás, a capacidade de produção é de até 100 milhões de doses. O acordo com o laboratório chinês prevê que, se a vacina for efetiva, o Brasil ficará com 60 milhões de doses para distribuição.
Este é o segundo teste de vacina contra a Covid-19 liberado pela Anvisa no país. No dia 2 de junho, a Agência autorizou o ensaio clínico da vacina desenvolvida pela Universidade de Oxford, no Reino Unido.


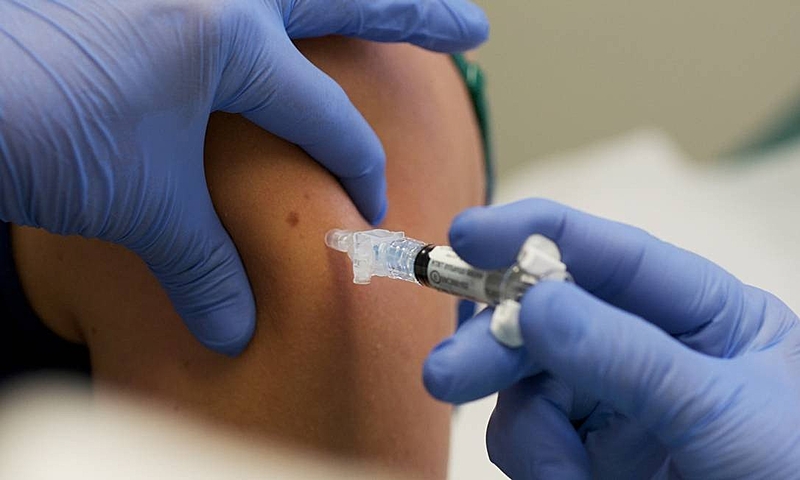

.png)




Adicionar comentário